SALUD
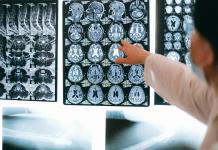
La anemia de Fanconi es una enfermedad rara que afecta a la médula ósea y predispone a padecer cáncer. La investigación en terapia génica ha abierto la puerta a la esperanza de una posible cura.
DESTACADOS.
- La enfermedad es muy compleja desde el punto de vista genético pues, hasta el momento, se han descrito 22 genes involucrados en ella.
- Si un hombre y una mujer que ambos sean portadores de mutaciones en un determinado gen implicado en la anemia de Fanconi tienen descendencia, poseen un 25% de probabilidades de tener un hijo sano no portador, un 50% de probabilidades de tener un hijo portador y un 25% de probabilidades de tener un hijo enfermo.
- El 90% de los casos de anemia de Fanconi se diagnostica antes de la adolescencia.
- La anemia de Fanconi está considerada una enfermedad rara pues afecta a una persona de cada 300 000. Daña la médula ósea, lo que tiene como consecuencia una menor producción de todos los tipos de células sanguíneas: glóbulos blancos, glóbulos rojos y plaquetas.
“La insuficiencia de glóbulos blancos puede conducir a infecciones; la falta de glóbulos rojos puede causar anemia y la disminución de la cantidad de plaquetas puede llevar a sangrados excesivos”
Detallan los especialistas del Centro de Información sobre Enfermedades Genéticas y Raras de Estados Unidos (GARD, por sus siglas en inglés).
Fue el pediatra suizo Guido Fanconi quien describió la enfermedad por primera vez en 1927. La anemia de Fanconi se caracteriza por malformaciones congénitas, déficit de células sanguíneas y alta predisposición a desarrollar cáncer.
“Las malformaciones más frecuentemente asociadas a la anemia de Fanconi son el retraso del crecimiento pre y postnatal, malformaciones renales, gastrointestinales, genitourinarias, cardíacas y esqueléticas, cabeza, ojos y boca pequeños, hipogonadismo, sordera parcial, anormalidades cutáneas como hiper o hipopigmentación, manchas `café con leche´ y elevados niveles de alfafetoproteína en sangre (un marcador tumoral).
Tres de cada diez pacientes, sin embargo, no presentan malformación alguna”, explica la Fundación Anemia de Fanconi.
“Cuando las malformaciones congénitas no son significativas, el diagnóstico puede retrasarse hasta la manifestación de las anomalías hematológicas. La insuficiencia medular aparece a una edad media de 7 años y el 90% de los pacientes desarrolla insuficiencia medular antes de los 40 años de edad.
Las primeras manifestaciones son la macrocitosis (muy temprana) y la trombocitopenia”, recoge Orphanet, el portal europeo de referencia sobre enfermedades raras y medicamentos huérfanos. La macrocitosis es el aumento del tamaño de los glóbulos rojos y la trombocitopenia, la escasez de plaquetas.
Las personas con anemia de Fanconi también tienen un riesgo alto de padecer cáncer. Las células humanas están expuestas a diferentes agresiones del entorno que pueden causar daños en su ADN, por lo que necesitan reparación constante.
En la anemia de Fanconi, la reparación celular no funciona correctamente por lo que estas lesiones se acumulan, lo que suele conducir a la aparición de cáncer.
La elevada predisposición al cáncer es “particularmente significativa en el caso de las células sanguíneas, por lo que pueden desarrollarse leucemias mieloides. En edades más avanzadas, también se observa un riesgo de tumores en otros tejidos, por ejemplo, ginecológico, de cabeza y cuello o hepático”, señala la Fundación Anemia de Fanconi.
Esta entidad subraya que la anemia de Fanconi es muy compleja desde el punto de vista genético pues, hasta el momento, se han descrito 22 genes involucrados en ella.
“La falta de función de cualquiera de estos 22 genes produce esencialmente la misma enfermedad”, expone.
Se trata de una enfermedad hereditaria recesiva. Esto significa que para que una persona tenga la enfermedad, las dos copias (tanto la que recibe por parte de su padre como la que le llega por parte de su madre) de alguno de los genes implicados en la anemia de Fanconi debe estar afectada (mutada con pérdida de función).
Quienes posean una copia funcional y otra mutada de uno de estos genes son portadores, pero no están enfermos. Según datos de la Fundación Anemia de Fanconi, se estima que hay un portador de la enfermedad por cada 300 habitantes.
De este modo, si un hombre y una mujer que ambos sean portadores de mutaciones en un determinado gen implicado en la anemia de Fanconi tienen descendencia, poseen un 25% de probabilidades de tener un hijo sano no portador (si heredase las dos copias funcionales); un 50% de probabilidades de tener un hijo portador (si heredase de uno de sus progenitores una copia funcional y del otro una mutada) y un 25% de probabilidades de tener un hijo enfermo (si heredase las dos copias mutadas).

La anemia de Fanconi se caracteriza por malformaciones congénitas, déficit de células sanguíneas y alta predisposición a desarrollar cáncer. Imagen de Freepik
El 90% de los casos de anemia de Fanconi se diagnostica antes de la adolescencia. “Los pacientes muestran recuentos anormalmente bajos de células sanguíneas, tanto de glóbulos rojos (anemia), como de glóbulos blancos (leucopenia) y de plaquetas (trombocitopenia).
La primera manifestación suele ser una trombocitopenia aislada en más de la mitad de los casos, en los que se observan petequias (pequeñas manchas en la piel que aparecen debido a la rotura de capilares sanguíneos), hematomas o episodios de sangrado nasal o gastrointestinal.
Posteriormente se hacen evidentes los signos de la anemia, sobre todo, palidez, astenia (sensación de cansancio y debilidad) y anorexia. La tendencia a padecer procesos infecciosos debida a la deficiencia de glóbulos blancos suele ser de aparición tardía”, explica la Fundación Josep Carreras contra la Leucemia.
Cuando la anemia y la trombocitopenia son intensas y sintomáticas, es necesario realizar transfusiones de glóbulos rojos y plaquetas. Pero la terapia definitiva para la enfermedad consiste en un trasplante de médula ósea.
La situación más favorable sería que el donante fuera un familiar compatible pero sólo una minoría de pacientes lo tiene por lo que, con frecuencia, se recurre a donantes no emparentados.
“Los mejores resultados se obtienen cuando el trasplante se realiza en edades tempranas y cuando el paciente ha recibido un número reducido de transfusiones”
Detallan los expertos de la Fundación Anemia de Fanconi.
El trasplante de médula ósea requiere un tratamiento de acondicionamiento con quimioterapia para prevenir las reacciones de rechazo y tiene riesgos asociados, tanto a corto como a largo plazo, lo que con frecuencia supone hospitalizaciones prolongadas.
Un ensayo clínico español ha demostrado por primera vez que la terapia génica puede resultar eficaz y segura en pacientes con esta enfermedad. Los resultados de este trabajo, publicados en la revista The Lancet, son fruto de más de 20 años de investigación preclínica y del seguimiento de los pacientes durante siete años.
Estos están afectados por el subtipo A de la anemia de Fanconi, causado por mutaciones en el gen FANCA.
El procedimiento consiste en extraer células madre de los pacientes, corregir el defecto genético ex vivo utilizando un vector lentiviral portador del gen FANCA, que previamente había desarrollado el equipo investigador.
Una vez corregido el defecto genético, las células se volvieron a infundir en los pacientes, como si se tratara de una autotransfusión, de modo que no tuvieron que recibir quimioterapia y pudieron abandonar el hospital 72 horas después.
“Tras siete años de seguimiento, hemos podido confirmar que la presencia de las células corregidas ha continuado aumentando en los pacientes hasta alcanzar niveles superiores al 90% en dos de ellos, lo que ha permitido detener e incluso mejorar el fallo medular”
Detalla Julián Sevilla, hematólogo del Hospital Infantil Niño Jesús de Madrid e investigador principal de los ensayos clínicos.
Otro estudio, este en fase preclínica, ha demostrado en modelos de ratón la eficacia de la terapia génica in vivo (administrada directamente por vena) para la anemia de Fanconi.
- En este trabajo, liderado por el San Raffaele Telethon Institute for Gene Therapy (SR-TIGET) de Milán (Italia) y publicado en la revista Nature, el vector lentiviral terapéutico se administró por vía intravenosa a ratones recién nacidos que padecían la enfermedad.
Como consecuencia, los investigadores observaron que una pequeña proporción de las células madre de la médula ósea enfermas mostraban corrección de su defecto genético. A partir de ese momento, las células corregidas se fueron expandiendo progresivamente en la médula ósea y en la sangre de los animales.
El doctor Juan Bueren, que ha participado en ambos estudios, explica que “el hecho de que en la anemia de Fanconi las células madre corregidas muestren ventaja proliferativa hace de esta enfermedad un modelo ideal para una novedosa terapia lentiviral in vivo.
Por ello, y gracias a nuestra experiencia en la enfermedad, comenzamos una colaboración con los investigadores del Instituto TIGET de Milán”.
“Los resultados obtenidos en este trabajo pionero abren nuevas perspectivas al tratamiento de enfermedades hematológicas, en particular de la anemia de Fanconi, mediante sistemas mucho más sencillos que los que actualmente se están utilizando, lo que permitiría extender la aplicación de la terapia a un mayor número de pacientes”
Apunta la doctora Paula Río, que también ha formado parte de los dos estudios.
- Del penal a las calles: las consignas que marcharán desde las cárceles de México este 8M- 07 marzo, 2026
- Dermatitis atópica, cómo evitarla- 07 marzo, 2026
- ‘Apps’ nutricionales: instrucciones de uso saludable- 07 marzo, 2026
 UDGTV
UDGTV Radio UdeG
Radio UdeG